In der Medizintechnikbranche ist die Erlangung der ISO 13485-Zertifizierung ein entscheidender Schritt, um Qualität und Compliance zu gewährleisten. Viele Unternehmen sind jedoch besorgt über die Kosten der ISO 13485-Zertifizierung und fragen sich, wie sie diese erhalten können, ohne das Budget zu sprengen. Dieser international anerkannte Standard legt strenge Anforderungen an Qualitätsmanagementsysteme fest, weshalb es für Hersteller unerlässlich ist, die finanziellen Auswirkungen zu verstehen, bevor sie den Weg der Zertifizierung einschlagen.
Der Prozess der ISO 13485-Zertifizierung umfasst mehrere Phasen, die jeweils zu den Gesamtkosten beitragen. Von der ersten Bewertung über die Implementierung bis hin zum finalen Audit müssen Unternehmen verschiedene Faktoren berücksichtigen, die die Gesamtausgaben beeinflussen. Dieser Artikel befasst sich eingehend mit den Schlüsselkomponenten der Kosten für eine ISO 13485-Zertifizierung, einschließlich der Gebühren von Zertifizierungsgesellschaften, der internen Ressourcenallokation und potenzieller versteckter Kosten. Zudem werden Strategien zur Optimierung des Zertifizierungsbudgets und zur Maximierung der Kapitalrendite (ROI) untersucht, um Organisationen, die ihre Qualitätsmanagementsysteme und ihren globalen Marktzugang verbessern möchten, wertvolle Einblicke zu bieten.
Was ist eine ISO 13485-Zertifizierung?
Definition
Die ISO 13485-Zertifizierung ist ein weltweit anerkannter Standard, der die Einhaltung der Anforderungen an ein Qualitätsmanagementsystem in der Medizintechnikbranche durch eine Organisation nachweist. Dieser von der Internationalen Organisation für Normung (ISO) festgelegte Standard gilt für Organisationen, die an verschiedenen Phasen des Lebenszyklus eines Medizinprodukts beteiligt sind, einschließlich Design, Entwicklung, Produktion, Lagerung, Vertrieb, Installation und Instandhaltung.
Die aktuelle Version, ISO 13485:2016, dient als Brücke zwischen regulatorischen Erwartungen und bewährten Branchenpraktiken (Best Practices). Sie bietet einen Rahmen für Medizintechnikunternehmen, um effektive Qualitätsmanagementsysteme (QMS) aufzubauen und aufrechtzuerhalten, die mit internationalen Richtlinien und regulatorischen Anforderungen übereinstimmen.
Bedeutung für Hersteller von Medizinprodukten
Für Hersteller von Medizinprodukten hat die ISO 13485-Zertifizierung eine signifikante Bedeutung:
-
Qualitätssicherung: Sie trägt dazu bei, die Produktion sicherer, zuverlässiger und wirksamer Medizinprodukte zu gewährleisten.
-
Einhaltung gesetzlicher Vorschriften (Regulatory Compliance): Die Zertifizierung hilft bei der Erfüllung verschiedener regulatorischer Anforderungen, einschließlich derer der US-amerikanischen Food and Drug Administration (FDA) und der Verordnungen der Europäischen Union (EU).
-
Marktzugang: Viele Länder und Regionen verlangen von Herstellern medizinischer Geräte eine ISO 13485-Zertifizierung für den Verkauf ihrer Produkte, was sie für den globalen Marktzugang unerlässlich macht.
-
Risikomanagement: Die Norm betont einen risikobasierten Ansatz im Qualitätsmanagement, der Organisationen hilft, potenzielle Probleme proaktiv zu identifizieren und zu mindern.
-
Wettbewerbsvorteil: Eine Zertifizierung kann einen Wettbewerbsvorteil verschaffen, da sie das Engagement für Qualität und Sicherheit demonstriert.
-
Kundenvertrauen: Sie stärkt die Glaubwürdigkeit und das Vertrauen bei Kunden, Partnern und Aufsichtsbehörden.
-
Kontinuierliche Verbesserung: Die Norm fördert die stetige Optimierung von Prozessen und Produkten.
Hauptanforderungen
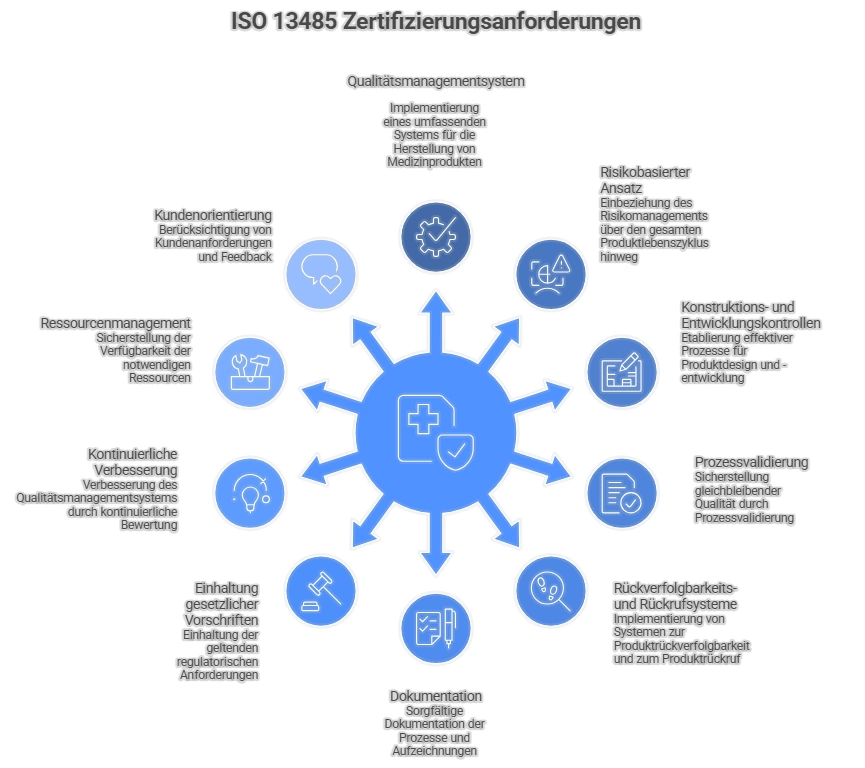
Die ISO 13485:2016 nennt mehrere Hauptanforderungen für Organisationen, die eine Zertifizierung anstreben:
-
Qualitätsmanagementsystem (QMS): Implementierung eines umfassenden QMS, das alle Aspekte der Herstellung von Medizinprodukten und damit verbundener Dienstleistungen abdeckt.
-
Risikobasierter Ansatz: Einbeziehung von Risikomanagement-Prinzipien über den gesamten Produktlebenszyklus hinweg.
-
Design- und Entwicklungslenkung: Etablierung von Prozessen für effektives Produktdesign und -entwicklung.
-
Prozessvalidierung: Validierung von Produktions- und Dienstleistungsprozessen zur Sicherstellung gleichbleibender Qualität.
-
Rückverfolgbarkeit und Rückrufsysteme: Implementierung von Systemen für eine effektive Produktrückverfolgbarkeit und das Management von Rückrufen.
-
Dokumentation: Führen einer gründlichen Dokumentation von Prozessen, Verfahren und Qualitätsaufzeichnungen.
-
Regulatorische Compliance: Sicherstellung der Einhaltung geltender regulatorischer Anforderungen in den Zielmärkten.
-
Kontinuierliche Verbesserung: Einrichtung von Mechanismen zur laufenden Bewertung und Verbesserung des QMS.
-
Ressourcenmanagement: Sicherstellung der Verfügbarkeit notwendiger Ressourcen, einschließlich geschultem Personal und Infrastruktur.
-
Kundenorientierung: Aufrechterhaltung von Prozessen, um auf Kundenanforderungen und Feedback einzugehen.
Durch die Erfüllung dieser Anforderungen können Organisationen ihr Engagement für Qualität, Sicherheit und regulatorische Compliance in der Medizintechnikbranche unter Beweis stellen. Die ISO 13485-Zertifizierung hilft Herstellern nicht nur bei der Produktion hochwertiger Produkte, sondern unterstützt auch ihre Bemühungen, sich in komplexen regulatorischen Landschaften zurechtzufinden und ihre globale Marktpräsenz auszubauen.
Faktoren, die die Kosten der ISO 13485-Zertifizierung beeinflussen
Die Kosten für die Erlangung einer ISO 13485-Zertifizierung können je nach mehreren Schlüsselfaktoren erheblich variieren. Das Verständnis dieser Elemente ist entscheidend für Organisationen, die planen, diesen international anerkannten Standard für Qualitätsmanagementsysteme in der Medizintechnikbranche anzustreben.
Unternehmensgröße
Die Größe einer Organisation spielt eine wesentliche Rolle bei der Bestimmung der ISO 13485-Zertifizierungskosten. Größere Unternehmen haben typischerweise höhere Ausgaben aufgrund von:
-
Implementierungsumfang: Größere Organisationen benötigen oft umfangreichere und komplexere Qualitätsmanagementsysteme.
-
Mitarbeiterzahl: Eine größere Belegschaft erfordert umfassendere Schulungen, Sensibilisierungsprogramme und interne Audittätigkeiten.
-
Ressourcenallokation: Größere Unternehmen müssen möglicherweise mehr Personal und finanzielle Mittel für den Zertifizierungsprozess bereitstellen.
Für kleinere Unternehmen oder solche mit begrenzten Budgets kann die für die ISO 13485-Zertifizierung erforderliche Ressourcenallokation eine besondere Herausforderung darstellen.
Komplexität der Betriebsabläufe
Der Umfang und die Komplexität der Betriebsabläufe einer Organisation wirken sich direkt auf die Zertifizierungskosten aus:
-
Operative Präsenz: Unternehmen mit mehreren Standorten oder Anlagen können höhere Kosten für die Implementierung und Aufrechterhaltung eines konsistenten Qualitätsmanagementsystems an allen Standorten haben.
-
Produktpalette: Ein breiteres Spektrum an Produkten und Aktivitäten, die unter die Norm fallen, kann zu erhöhten Investitionen in Ressourcen und Prozesse führen.
-
Prozesskomplexität: Selbst kleinere Unternehmen mit komplexen Verfahren können mit höheren Zertifizierungsgebühren konfrontiert sein.
Aktueller Status des Qualitätsmanagementsystems
Der Zustand des bestehenden Qualitätsmanagementsystems (QMS) einer Organisation hat einen erheblichen Einfluss auf die Gesamtkosten:
-
Systemreife: Unternehmen, die bereits über ein robustes QMS verfügen, empfinden den Zertifizierungsprozess möglicherweise als geradliniger und kostengünstiger.
-
Ausrichtung an ISO 13485: Der Grad, in dem das aktuelle System bereits mit den Anforderungen der ISO 13485 übereinstimmt, beeinflusst den Umfang der erforderlichen Anpassungen.
-
Gap-Analyse (Lückenanalyse): Organisationen, die bei Null anfangen oder signifikante Compliance-Lücken aufweisen, müssen mit höheren Kosten für Systementwicklung und -implementierung rechnen.
Geografischer Standort
Der geografische Kontext einer Organisation kann die Zertifizierungskosten auf verschiedene Weise beeinflussen:
-
Regionale Unterschiede: In verschiedenen Regionen können unterschiedliche Sätze für Berater und Auditoren gelten, die bei Zertifizierungsaudits unterstützen.
-
Betrachtung mehrerer Standorte: Organisationen mit mehreren Standorten können aufgrund der Notwendigkeit von Audits an jedem Standort höhere Kosten haben.
-
Lokale Marktfaktoren: Die Kosten für Zertifizierungsstellen und damit verbundene Dienstleistungen können je nach lokalen Marktbedingungen variieren.
Es ist wichtig zu beachten, dass diese Faktoren zwar die Kosten erheblich beeinflussen, aber auch die umfassende Natur der ISO 13485-Zertifizierung widerspiegeln. Die Investition in diesen Prozess gewährleistet nicht nur die Einhaltung internationaler Standards, sondern demonstriert auch ein Engagement für Qualität und Sicherheit in der Medizintechnikbranche.
Organisationen, die eine ISO 13485-Zertifizierung anstreben, sollten diese Faktoren sorgfältig bewerten und in Erwägung ziehen, Zertifizierungsstellen oder Branchenexperten zu konsultieren, um genaue Kostenschätzungen zu erhalten. Durch das Verständnis dieser Einflussfaktoren können sich Unternehmen besser auf den Zertifizierungsprozess vorbereiten und Ressourcen effektiv zuweisen, um diesen wertvollen Industriestandard zu erreichen.
Aufschlüsselung der ISO 13485-Zertifizierungskosten
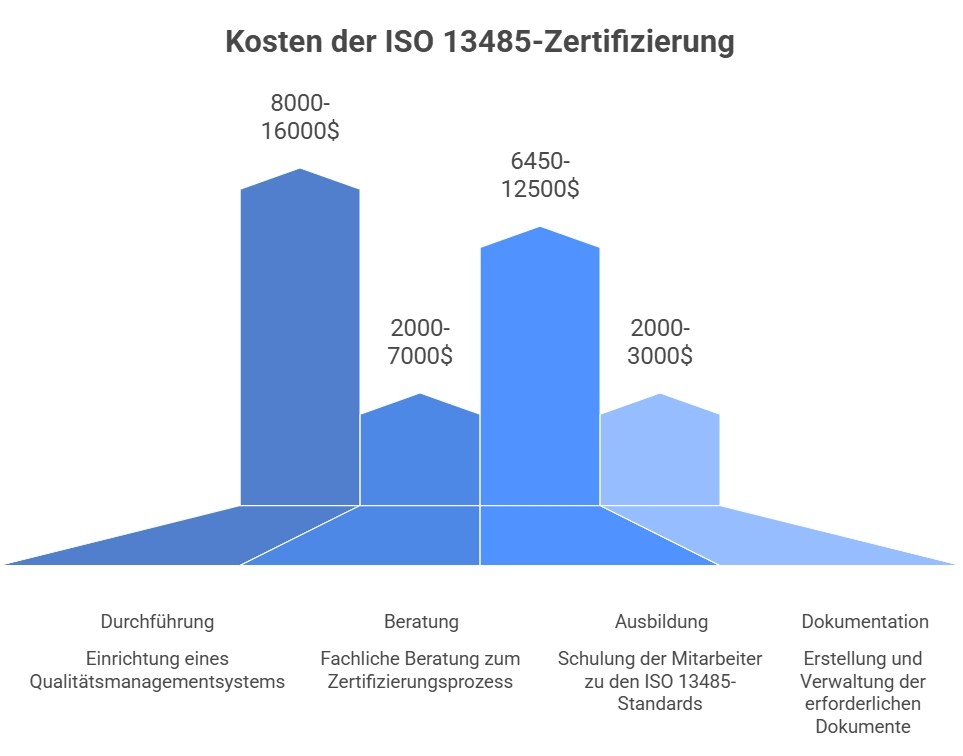
Die Kosten der ISO 13485-Zertifizierung setzen sich aus verschiedenen Komponenten zusammen, die Organisationen bei der Budgetierung für diesen wichtigen Qualitätsmanagementstandard berücksichtigen müssen. Das Verständnis dieser Kosten hilft Unternehmen, effektiv zu planen und Ressourcen angemessen zuzuweisen. Die Aufschlüsselung der ISO 13485-Zertifizierungskosten umfasst typischerweise Implementierungskosten, Beraterhonorare, Schulungsausgaben und Dokumentationskosten.
Implementierungskosten
Implementierungskosten machen einen erheblichen Teil der Gesamtausgaben für die ISO 13485-Zertifizierung aus. Diese Kosten stehen im Zusammenhang mit der Einrichtung eines ISO 13485-konformen Qualitätssystems und dessen vollständiger Implementierung innerhalb der Organisation. Der Implementierungsprozess kann zeitaufwändig und ressourcenintensiv sein und oft mehrere Monate in Anspruch nehmen.
Für kleine Unternehmen können die Implementierungskosten zwischen 8.000 $ und 16.000 $ liegen, je nachdem, ob die Arbeit extern (offsite) oder vor Ort (onsite) durchgeführt wird. Größere Organisationen oder solche mit komplexeren Abläufen können mit höheren Implementierungskosten konfrontiert sein, die potenziell bis zu 25.000 $ oder mehr erreichen.
Beraterhonorare
Viele Organisationen entscheiden sich dafür, externe Berater zu engagieren, die sie durch den Zertifizierungsprozess führen. Die Beraterhonorare können je nach Expertise und Reputation des Beratungsunternehmens variieren. Diese Fachleute unterstützen bei verschiedenen Aspekten des Zertifizierungsprozesses, darunter:
-
Erstellung von Qualitätshandbüchern und verbindlichen Verfahrensanweisungen
-
Implementierungsplanung
-
Erstellung von Organigrammen und Definition von Verantwortlichkeiten
-
Erläuterung von Normklauseln für Prozesseigner
-
Durchführung interner Audits
-
Unterstützung während der Audits durch Zertifizierungsstellen
Beraterhonorare können zwischen 2.000 $ und 4.000 $ für externe Arbeit und zwischen 7.000 $ und 11.000 $ für Unterstützung vor Ort liegen, abhängig von der Größe und Komplexität der Organisation.
Schulungsausgaben
Schulungen sind ein entscheidender Aspekt der ISO 13485-Zertifizierung, um sicherzustellen, dass die Mitarbeiter das Qualitätsmanagementsystem verstehen und effektiv umsetzen können. Zu den Schulungsausgaben können gehören:
-
Entwicklung von Schulungsmaterialien
-
Trainerhonorare
-
Arbeitszeit der Mitarbeiter für Schulungssitzungen
-
Seminare und Sensibilisierungskampagnen
Organisationen sollten ein Budget für fortlaufende Schulungen einplanen, um Compliance und kontinuierliche Verbesserung aufrechtzuerhalten.
Typische Marktkosten für Schulungen:
Obwohl die Kosten je nach Anbieter und Format variieren, können Sie mit folgenden Richtwerten kalkulieren:
-
E-Learning / Online-Selbstlernkurse: Ideal für die allgemeine Sensibilisierung der Mitarbeiter. Die Kosten liegen oft zwischen 150 $ und 500 $ pro Teilnehmer.
-
Öffentliche Seminare (Präsenz oder virtuell): Für spezifischere Rollen (z. B. Qualitätsmanager). Hier liegen die Preise meist zwischen 800 $ und 1.500 $ pro Teilnehmer für 1- bis 2-tägige Kurse.
-
Qualifikation zum Internen Auditor: Eine wesentliche Rolle im QM-System. Rechnen Sie mit ca. 1.000 $ bis 2.000 $ pro Teilnehmer.
-
Lead-Auditor-Schulung: Eine umfassende, meist 5-tägige Ausbildung. Die Kosten belaufen sich auf ca. 2.500 $ bis 4.000 $ pro Person.
-
Inhouse-Schulungen: Für Gruppen ab 5 Personen oft die wirtschaftlichste Lösung. Ein Trainer führt die Schulung (virtuell oder vor Ort) durch. Tagessätze für Trainer liegen typischerweise zwischen 2.000 $ und 4.500 $ (zzgl. Reisekosten), decken aber die Schulung des gesamten Teams ab.
Dokumentationskosten
Die Dokumentation ist ein kritisches Element der ISO 13485-Zertifizierung. Organisationen müssen eine umfassende Dokumentation entwickeln und pflegen, einschließlich:
-
Qualitätsmanagement-Handbuch
-
Verbindliche Verfahrensanweisungen
-
Wichtige Formulare und Vorlagen
-
Prozessdokumentation
-
Aufzeichnungen und Berichte
Die Kosten für die Dokumentationsentwicklung können zwischen 2.000 $ und 3.000 $ liegen, hauptsächlich für externe Arbeit. Dies umfasst das Entwerfen des Qualitätshandbuchs, der verbindlichen Verfahren und wesentlicher Formulare, was typischerweise 15 bis 20 Arbeitstage in Anspruch nimmt.
Es ist wichtig zu beachten, dass die Gesamtkosten der ISO 13485-Zertifizierung erheblich variieren können, basierend auf Faktoren wie Unternehmensgröße, operativer Komplexität und dem Status des aktuellen Qualitätsmanagementsystems. Organisationen sollten auch laufende Kosten für die Aufrechterhaltung der Zertifizierung berücksichtigen, die sich jährlich typischerweise auf etwa ein Drittel der ursprünglichen Zertifizierungskosten belaufen.
Um Kosten zu optimieren, können Unternehmen eine Kombination aus externer und Vor-Ort-Arbeit in Betracht ziehen, da externe Aktivitäten in der Regel geringere Ausgaben verursachen. Zudem können Organisationen mit interner Expertise möglicherweise Beraterhonorare reduzieren, indem sie einige Aspekte des Zertifizierungsprozesses intern abwickeln.
Gebühren für Auditierung und Zertifizierungsstellen
Gebühren für Auditierung und Zertifizierungsstellen machen einen signifikanten Teil der ISO 13485-Zertifizierungskosten aus. Diese Gebühren werden an externe Zertifizierungsstellen (auch als Registrare bekannt) für ihre Dienstleistungen zur Bewertung und Zertifizierung des Qualitätsmanagementsystems einer Organisation gezahlt. Die Kosten können basierend auf Faktoren wie dem Geschäftsumfang, der Glaubwürdigkeit der Zertifizierungsstelle und der Komplexität der Betriebsabläufe der Organisation variieren.
Erstzertifizierungsaudit
Das Erstzertifizierungsaudit ist eine umfassende Bewertung des Qualitätsmanagementsystems einer Organisation zur Sicherstellung der Einhaltung der ISO 13485-Standards. Dieser Prozess umfasst typischerweise zwei Stufen:
-
Audit Stufe 1 (Dokumentenprüfung): Diese erste Bewertung prüft die Dokumentation der Organisation und die Bereitschaft zur Zertifizierung. Die Kosten für diese Stufe können zwischen 500 $ und 1.000 $ liegen, je nachdem, ob die Zertifizierungsstelle akkreditiert oder nicht akkreditiert ist.
-
Audit Stufe 2 (Zertifizierungsaudit): Dies ist eine tiefgehende Bewertung der Prozesse der Organisation und der Implementierung des Qualitätsmanagementsystems. Die Gebühren für diese Stufe können erheblich variieren und reichen von 1.000 $ für nicht akkreditierte Stellen bis zu 3.000 $ für akkreditierte.
Nach erfolgreichem Abschluss beider Stufen stellt die Zertifizierungsstelle das ISO 13485-Zertifikat aus. Die Gebühr für die Ausstellung des Zertifikats liegt typischerweise zwischen 500 $ und 1.000 $.
Es ist wichtig zu beachten, dass diese Zahlen auf kleinen Unternehmen mit weniger als 10 Mitarbeitern basieren. Für größere Organisationen kann eine zusätzliche Gebühr von etwa 500 $ pro weiteren 10 Mitarbeitern anfallen.
Überwachungsaudits
Die ISO 13485-Zertifizierung erfordert jährliche Überwachungsaudits, um die fortlaufende Einhaltung des Standards sicherzustellen. Diese Audits sind weniger umfangreich als das Erstzertifizierungsaudit, aber entscheidend für die Aufrechterhaltung der Gültigkeit der Zertifizierung. Wichtige Punkte zu Überwachungsaudits sind:
-
Häufigkeit: Überwachungsaudits werden typischerweise jährlich während des dreijährigen Zertifizierungszyklus durchgeführt.
-
Kosten: Die Gebühren für Überwachungsaudits liegen in der Regel 25–35 % unter den Kosten des Erstzertifizierungsaudits, da das Qualitätsmanagementsystem bereits etabliert ist.
-
Umfang: Diese Audits konzentrieren sich darauf zu verifizieren, dass die Organisation die Anforderungen der ISO 13485 konsequent erfüllt und ihre Prozesse weiter verbessert.
Rezertifizierungsaudits
Nach der ersten dreijährigen Zertifizierungsperiode müssen sich Organisationen einem Rezertifizierungsaudit unterziehen, um ihre ISO 13485-Zertifizierung zu erneuern. Dieser Prozess ähnelt dem Erstzertifizierungsaudit, kann jedoch gestrafft werden, wenn die Organisation eine konsistente Compliance aufrechterhalten hat. Wichtige Aspekte von Rezertifizierungsaudits sind:
-
Zeitpunkt: Rezertifizierungsaudits finden am Ende des dreijährigen Zertifizierungszyklus statt.
-
Umfang: Diese Audits sind umfassend und überprüfen das gesamte Qualitätsmanagementsystem, um fortgesetzte Compliance und Wirksamkeit sicherzustellen.
-
Kosten: Gebühren für Rezertifizierungsaudits ähneln oft den Kosten des Erstzertifizierungsaudits, da sie eine gründliche Bewertung der Organisationsprozesse beinhalten.
Es ist erwähnenswert, dass einige Zertifizierungsstellen möglicherweise nicht zwischen Zertifizierungs-, Überwachungs- und Rezertifizierungsaudits hinsichtlich der Anzahl der Audittage und der berechneten Gebühren unterscheiden. So berichtete beispielsweise ein Unternehmen, dass ihm etwa 5.250 $ pro Audittag für 7,5 Tage berechnet wurden, was insgesamt etwa 40.000 $ pro Jahr für Audits ausmachte, die CE-Kennzeichnung, ISO 13485:2016 und MDSAP (Medical Device Single Audit Program) abdeckten.
Organisationen, die eine ISO 13485-Zertifizierung anstreben, sollten ihre Optionen bei der Auswahl einer Zertifizierungsstelle sorgfältig abwägen. Es ist ratsam, mehrere akkreditierte Zertifizierungsstellen zu kontaktieren, deren Auditgebühren und Prozesse zu vergleichen und eine auszuwählen, die am besten zu den Bedürfnissen und dem Budget der Organisation passt. Während nicht akkreditierte Zertifizierungsstellen möglicherweise niedrigere Gebühren anbieten, sind Zertifikate von akkreditierten Stellen in der Branche im Allgemeinen angesehener und wertvoller.
Versteckte Kosten, die zu berücksichtigen sind
Bei der Verfolgung einer ISO 13485-Zertifizierung müssen sich Organisationen mehrerer versteckter Kosten bewusst sein, die ihr Budget erheblich belasten können. Diese Kosten gehen oft über die anfänglichen Zertifizierungsgebühren hinaus und können langfristige Auswirkungen auf die Ressourcen und den Betrieb des Unternehmens haben.
Interne Ressourcenallokation
Einer der primären versteckten Kostenfaktoren im Zusammenhang mit der ISO 13485-Zertifizierung ist die Zuweisung interner Ressourcen. Dies beinhaltet den Einsatz von Mitarbeiterzeit und Arbeitskraft für verschiedene Aspekte des Zertifizierungsprozesses:
-
Dokumentationsentwicklung: Die Erstellung und Pflege einer umfassenden Dokumentation für das Qualitätsmanagementsystem erfordert viel Zeit und Fachwissen.
-
Schulung: Mitarbeiter benötigen gründliche Schulungen zu neuen Prozessen und Verfahren, was zeitaufwändig sein kann und zusätzliche Ressourcen erfordern kann.
-
Interne Audits: Organisationen sollten regelmäßig interne Audits durchführen, idealerweise mindestens einmal jährlich. Diese Audits helfen, Verbesserungsbereiche zu identifizieren und die Einhaltung der ISO 13485-Standards sicherzustellen.
-
Managementbewertungen: Die ISO 13485 verlangt geplante Managementbewertungen (Reviews), um sicherzustellen, dass die Verfahren des Qualitätsmanagementsystems mit der Qualitätspolitik des Unternehmens übereinstimmen. Diese Bewertungen können zeitintensiv sein und erfordern sorgfältige Vorbereitung.
Unternehmen, denen interne Expertise im Bereich Qualitätsmanagementsysteme fehlt, müssen möglicherweise externe Berater oder Trainer engagieren, was die Kosten weiter erhöht. Auch der Reifegrad des bestehenden Qualitätsmanagementsystems beeinflusst die für die Implementierung erforderlichen Ressourcen.
Potenzielle Betriebsunterbrechungen
Die Implementierung der ISO 13485 kann zu vorübergehenden Betriebsunterbrechungen führen, die finanzielle Auswirkungen haben können:
-
Produktivitätsverluste: Während sich Mitarbeiter an neue Prozesse anpassen und Schulungen durchlaufen, kann es zu einem vorübergehenden Rückgang der Produktivität kommen.
-
Prozessänderungen: Die Anpassung bestehender Arbeitsabläufe an die Anforderungen der ISO 13485 kann kurzfristige Störungen im Betrieb verursachen.
-
Zeitliche Überlegungen: Das überhastete Durchlaufen des Zertifizierungsprozesses zur Einhaltung von Fristen kann zu Ineffizienzen und Fehlern führen, was potenziell zusätzliche Ausgaben nach sich zieht.
-
Kultureller Wandel: Die Einführung einer qualitätsorientierten Denkweise im gesamten Unternehmen kann Zeit und Mühe erfordern, um etablierte Praktiken und Einstellungen zu ändern.
Laufende Wartungskosten
Das Erreichen der ISO 13485-Zertifizierung ist kein einmaliges Ereignis; es erfordert fortlaufendes Engagement und Ressourcen, um die Compliance aufrechtzuerhalten:
-
Jährliche Überwachungsaudits: Diese Audits stellen die fortgesetzte Einhaltung der ISO 13485-Standards sicher und kosten typischerweise etwa ein Drittel der ursprünglichen Zertifizierungsgebühr.
-
Rezertifizierung: Alle drei Jahre müssen sich Organisationen einem umfassenden Rezertifizierungsaudit unterziehen, das in Umfang und Kosten dem ursprünglichen Zertifizierungsprozess ähneln kann.
-
Kontinuierliche Verbesserung: Die ISO 13485 betont die stetige Verbesserung von Prozessen und Produkten, was zusätzliche Investitionen in Technologie, Schulung oder Ressourcen erfordern kann.
-
Dokumentenmanagement: Die Pflege und Aktualisierung der Dokumentation ist ein kontinuierlicher Prozess, der Zeit und Aufmerksamkeit der Mitarbeiter verlangt.
-
Korrektur- und Vorbeugungsmaßnahmen (CAPA): Die Implementierung und Verwaltung von CAPA-Verfahren ist kritisch für die Compliance und kann signifikante laufende Ressourcen binden.
-
Lieferantenmanagement: Die Bewertung und das Management von Lieferantenrisiken ist ein fortlaufender Prozess, der zusätzliche Kosten und Ressourcen verursachen kann.
-
Kundenfeedback-Systeme: Die Einrichtung und Wartung von Systemen zur Erfassung und Bearbeitung von Kundenfeedback ist für die ISO 13485-Compliance wesentlich und kann laufende Kosten verursachen.
Durch die Berücksichtigung dieser versteckten Kosten können sich Organisationen besser auf die finanziellen und operativen Auswirkungen der ISO 13485-Zertifizierung vorbereiten. Obwohl diese Ausgaben entmutigend wirken mögen, ist es wichtig, sie als Investitionen in Qualität und Effizienz zu betrachten, die zu langfristigen Vorteilen führen können, einschließlich verbesserter Produktqualität, erhöhter Kundenzufriedenheit und gesteigerter Wettbewerbsfähigkeit in der Medizintechnikbranche.
Kostensparende Strategien für die ISO 13485-Zertifizierung
Selbstimplementierung vs. Einstellung eines Beraters
Organisationen, die eine ISO 13485-Zertifizierung anstreben, haben zwei Hauptoptionen: Selbstimplementierung oder die Beauftragung eines Beraters. Jeder Ansatz hat seine Vorzüge und potenziellen Kostenauswirkungen.
Die Selbstimplementierung beinhaltet den Aufbau von Fähigkeiten und Kompetenzen des vorhandenen Personals. Diese Strategie kann kostengünstiger sein als das Outsourcing an Berater. Durch die Bereitstellung notwendiger Schulungen für das Team befähigen Organisationen ihre Mitarbeiter, das Qualitätsmanagementsystem (QMS) effektiv zu implementieren und zu verwalten. Dieser Ansatz reduziert nicht nur die unmittelbaren Kosten, sondern stärkt auch das Personal bei der Vorbereitung auf das Zertifizierungsaudit, was das Risiko von Non-Compliance minimiert, die zusätzliche Audits erforderlich machen könnte.
Die Beauftragung eines ISO-Zertifizierungsberaters bringt jedoch mehrere Vorteile mit sich:
-
Expertise: Berater verfügen über umfassendes Wissen und Erfahrung im ISO-Zertifizierungsprozess, was diesen schneller und reibungsloser macht.
-
Objektivität: Sie bringen eine frische Perspektive ein und identifizieren Verbesserungsbereiche, die internes Personal möglicherweise übersehen würde.
-
Zeitersparnis: Berater übernehmen einen Großteil der komplexen Arbeit, sodass sich die Organisation auf ihre Kernaktivitäten konzentrieren kann.
-
Verbesserte Effizienz: Mit ihrem tiefgehenden Verständnis der Norm können Berater den Zertifizierungsprozess straffen.
-
Erhöhte Erfolgschancen: Ihre Erfahrung kann die Wahrscheinlichkeit eines erfolgreichen Zertifizierungsergebnisses erhöhen.
Während Beraterhonorare zwischen 100 $ und 300 $ pro Stunde liegen können, mit Gesamtprojektkosten von potenziell 10.000 $ bis 100.000 $, kann sich die Investition für Organisationen lohnen, denen interne Expertise fehlt oder die unter Zeitdruck stehen.
Gruppenschulungen
Gruppenschulungen bieten eine kosteneffiziente Möglichkeit, interne Kompetenzen aufzubauen. Diese Sitzungen können zwischen 500 $ und 2.000 $ kosten und stellen eine erschwinglichere Option im Vergleich zu Einzelschulungen oder umfangreichen Beratungsdiensten dar.
Zu den Hauptvorteilen von Gruppenschulungen gehören:
-
Gemeinsame Lernerfahrungen
-
Gelegenheit für Teamdiskussionen und Problemlösung
-
Konsistentes Verständnis der ISO 13485-Anforderungen im gesamten Unternehmen
Organisationen können verschiedene Schulungsoptionen prüfen, darunter:
-
Kurse zu den Anforderungen der ISO 13485:2016
-
Schulung zum internen Auditor
-
Zertifizierungsprogramme für Lead Auditoren
Diese Kurse vermitteln umfassendes Wissen über Konzepte, Richtlinien und Anforderungen der ISO 13485 und statten Mitarbeiter mit den notwendigen Werkzeugen aus, um das QMS effektiv zu implementieren und aufrechtzuerhalten.
Phasenweiser Implementierungsansatz
Ein phasenweiser Implementierungsansatz kann Organisationen helfen, Kosten und Ressourcen effektiver zu verwalten. Diese Strategie beinhaltet die Aufteilung des Zertifizierungsprozesses in überschaubare Stufen, was eine bessere Budgetallokation und reduzierte Störungen des Tagesgeschäfts ermöglicht.
Ein effektives Modell ist das „14-Stufen-Programm zur Implementierung und Zertifizierung eines Qualitätsmanagementsystems“, das einen Rahmen bietet, um Systeme zu entwickeln oder zu harmonisieren, die FDA- und/oder ISO 13485-Anforderungen erfüllen. Für kleinere Unternehmen oder solche in frühen Produktentwicklungsphasen kann ein „Quick-Start“-QMS-Entwicklungsprogramm geeigneter sein, das sich auf die Etablierung von QMS-Elementen konzentriert, die für die aktuellen Fertigungsanforderungen angemessen sind.
Ein typischer phasenweiser Ansatz umfasst:
-
Phase I: Gap-Analyse und Aktionsplanung
-
Bewertung des aktuellen Compliance-Niveaus
-
Identifizierung von Verbesserungsmöglichkeiten
-
Entwicklung eines Aktionsplans
-
-
Phase II: Umsetzung des Aktionsplans
-
Ausführung der in Phase I skizzierten Schritte
-
Durchführung interner Audits
-
Vorbereitung auf das Zertifizierungsaudit
-
Dieser Ansatz ermöglicht es Organisationen, Kosten über die Zeit zu verteilen und Ressourcen effizienter zuzuweisen. Er bietet auch die Möglichkeit, interne Expertise schrittweise aufzubauen, was die Abhängigkeit von externen Beratern im Verlauf der Implementierung verringert.
Durch die Nutzung dieser kostensparenden Strategien können Organisationen die ISO 13485-Zertifizierung verfolgen, ohne übermäßige Ausgaben zu tätigen. Der Schlüssel liegt in sorgfältiger Planung, strategischer Ressourcenallokation und dem Engagement, interne Kompetenzen aufzubauen. Während der Zertifizierungsprozess Investitionen erfordert, können diese Ansätze Organisationen helfen, Compliance effizient und nachhaltig zu erreichen und letztendlich ihre Wettbewerbsfähigkeit in der Medizintechnikbranche zu stärken.
ROI der ISO 13485-Zertifizierung
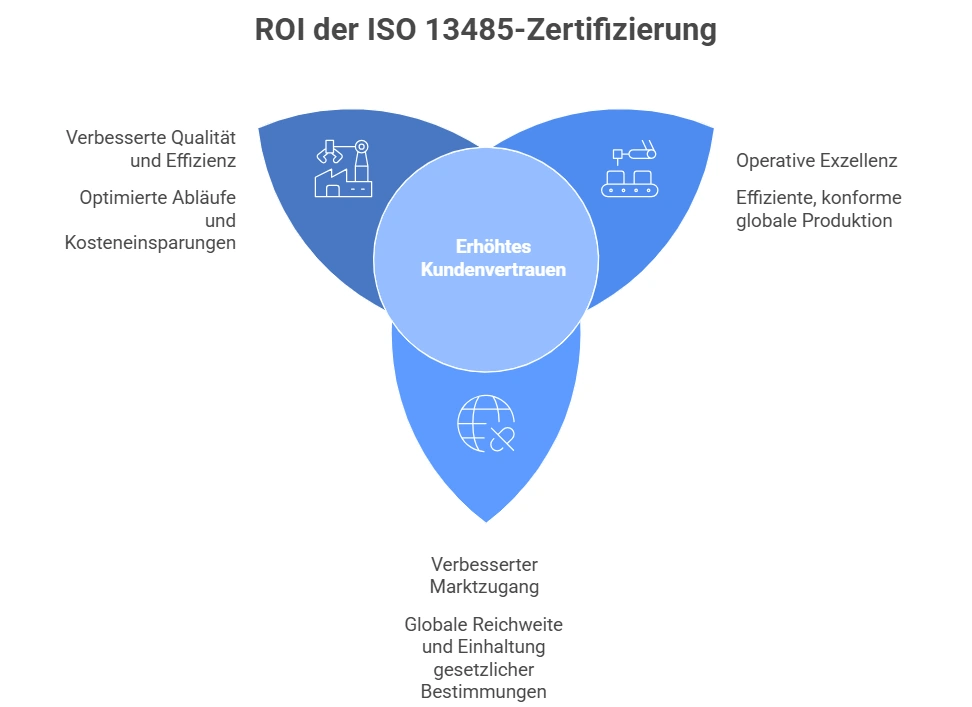
Die ISO 13485-Zertifizierung bietet Herstellern von Medizinprodukten erhebliche Investitionsrenditen (ROI). Dieser international anerkannte Standard bietet einen Rahmen für Qualitätsmanagementsysteme, der die Produktqualität verbessert, die Einhaltung gesetzlicher Vorschriften sicherstellt und den globalen Marktzugang erleichtert. Der ROI der ISO 13485-Zertifizierung manifestiert sich auf verschiedene Weisen, einschließlich verbesserter Qualität und Effizienz, erweitertem Marktzugang und erhöhtem Kundenvertrauen.
Verbesserte Qualität und Effizienz
Die ISO 13485-Zertifizierung rückt Qualität und kontinuierliche Verbesserung in den Mittelpunkt von Medizintechnikunternehmen. Durch die Implementierung eines robusten Qualitätsmanagementsystems können Unternehmen ihre Abläufe straffen und die Gesamteffizienz verbessern. Dies führt zu mehreren greifbaren Vorteilen:
-
Reduzierte Kosten: ISO 13485:2016 kann helfen, Verschwendung, Nacharbeit und andere Ineffizienzen zu minimieren und dadurch die Gesamtausgaben einer Organisation zu senken.
-
Erhöhte betriebliche Effizienz: Die Norm verlangt von Organisationen, umfassende Qualitätsmanagementsysteme einzurichten und aufrechtzuerhalten, die eine gleichbleibende Produktqualität sicherstellen und Risiken minimieren. Dies strafft Prozesse und verbessert interne Abläufe.
-
Kultur der kontinuierlichen Verbesserung: Die ISO 13485-Zertifizierung fördert eine Kultur der stetigen Optimierung und ermutigt Mitarbeiter, nach neuen Wegen zur Verbesserung von Produkten und Prozessen zu suchen.
-
Risikomanagement: Die Zertifizierung betont einen risikobasierten Ansatz, der es Organisationen ermöglicht, Risiken im Zusammenhang mit ihren Medizinprodukten effektiver zu identifizieren und zu steuern.
Durch die Einhaltung der ISO 13485-Richtlinien können Hersteller ihre Produktqualität und betriebliche Effizienz erheblich verbessern, was zu langfristigen Kosteneinsparungen und verbesserter Wettbewerbsfähigkeit führt.
Erweiterter Marktzugang
Die ISO 13485-Zertifizierung spielt eine entscheidende Rolle bei der Erweiterung der Marktchancen für Hersteller von Medizinprodukten. Die weltweite Anerkennung der Zertifizierung erleichtert den Eintritt in verschiedene Märkte und hilft Unternehmen, regulatorische Anforderungen zu erfüllen. Zu den Hauptvorteilen gehören:
-
Globaler Marktzugang: Viele Länder verlangen eine ISO 13485-Zertifizierung für Hersteller von Medizinprodukten, damit diese ihre Produkte legal innerhalb ihrer Grenzen verkaufen dürfen. Die Zertifizierung vereinfacht den Prozess zur Erlangung regulatorischer Zulassungen und hilft Organisationen, neue Märkte zu erschließen.
-
Regulatorische Compliance: Die ISO 13485 ist mit verschiedenen regulatorischen Rahmenbedingungen harmonisiert, wie etwa der Quality System Regulation (QSR) der FDA in den Vereinigten Staaten und der Medizinprodukteverordnung (MDR) der Europäischen Union. Diese Angleichung hilft Herstellern, die Einhaltung dieser Anforderungen nachzuweisen und regulatorischen Änderungen voraus zu sein.
-
Wettbewerbsvorteil: Die Zertifizierung unterscheidet Organisationen von Wettbewerbern, die diesen Nachweis möglicherweise nicht besitzen, und zeigt ihr Engagement für hohe Standards und Qualitätsmanagement.
-
Lieferantenbeziehungen: Zertifizierte Organisationen werden von Lieferanten und Partnern positiver wahrgenommen, was zu robusteren und verlässlicheren Lieferkettenbeziehungen führt.
Durch das Erreichen der ISO 13485-Zertifizierung können Hersteller von Medizinprodukten ihre globale Reichweite ausdehnen und sich als glaubwürdige Akteure auf dem internationalen Markt positionieren.
Erhöhtes Kundenvertrauen
Die ISO 13485-Zertifizierung dient als glaubwürdige und unabhängige Bestätigung des Engagements eines Medizinprodukteherstellers für Qualitätsmanagement. Diese Zertifizierung baut Vertrauen bei Kunden und anderen Interessengruppen auf verschiedene Weise auf:
-
Demonstriertes Engagement für Qualität: Die Zertifizierung liefert den Beweis für die Fähigkeit einer Organisation, konsequent hochwertige Produkte zu liefern, die Kunden- und regulatorische Anforderungen erfüllen.
-
Verbesserte Reputation und Glaubwürdigkeit: Die Akkreditierung nach ISO 13485:2016 zeigt Kunden, Lieferanten und anderen Stakeholdern, dass eine Organisation Qualität und Sicherheit ernst nimmt.
-
Verbesserte Kundenzufriedenheit: Die Norm enthält Anforderungen an Kundenfeedback und Beschwerdemanagement, was dazu beiträgt, den Kundenservice zu verbessern und die Loyalität zu steigern.
-
Transparenz und Rechenschaftspflicht: Die Implementierung eines Qualitätsmanagementsystems auf Basis der ISO 13485 erhöht Transparenz und Rechenschaftspflicht, was hilft, Vertrauen bei Stakeholdern aufzubauen.
-
Fokus auf Patientensicherheit: Durch die Befolgung der ISO 13485-Anforderungen können Organisationen sicherstellen, dass ihre Produkte nach höchsten Qualitätsstandards entwickelt und hergestellt werden, was das Risiko von Defekten oder Ausfällen reduziert und die Patientensicherheit verbessert.
Zusammenfassend lässt sich sagen, dass der ROI der ISO 13485-Zertifizierung über finanzielle Gewinne hinausgeht. Er umfasst verbesserte Qualität und Effizienz, erweiterten Marktzugang und erhöhtes Kundenvertrauen. Diese Vorteile tragen gemeinsam zum langfristigen Erfolg und Wachstum in der wettbewerbsintensiven Medizintechnikbranche bei.
Fazit
Die ISO 13485-Zertifizierung stellt eine bedeutende Investition für Hersteller von Medizinprodukten dar, doch ihre Vorteile überwiegen die Kosten bei weitem. Durch die Implementierung eines robusten Qualitätsmanagementsystems können Unternehmen ihre betriebliche Effizienz steigern, Risiken reduzieren und die Produktqualität verbessern. Dieses Engagement für Exzellenz öffnet Türen zu globalen Märkten, verschafft zertifizierten Organisationen einen Wettbewerbsvorteil und fördert das Vertrauen bei Kunden und Stakeholdern.
Da sich die Medizintechnikbranche ständig weiterentwickelt, dient die ISO 13485-Zertifizierung als Grundpfeiler für den Erfolg, indem sie die Einhaltung regulatorischer Anforderungen sicherstellt und eine Kultur der kontinuierlichen Verbesserung fördert. Ihr Einfluss auf Qualität, Marktzugang und Kundenvertrauen macht sie zu einem unschätzbaren Gut für Organisationen, die im Medizintechniksektor nach Exzellenz streben. Sind Sie bereit, Ihr Qualitätsmanagement zu verbessern? Kontaktieren Sie uns jetzt und lassen Sie uns besprechen, wie wir zusammenarbeiten können, um Ihre ISO-Zertifizierungsziele zu erreichen.
FAQs:
Was ist ISO 13485?
ISO 13485 ist eine Norm, die speziell für Organisationen entwickelt wurde, die an Design, Produktion, Installation und Instandhaltung von Medizinprodukten sowie damit verbundenen Dienstleistungen beteiligt sind. Sie dient zudem als Leitlinie für interne und externe Parteien, wie beispielsweise Zertifizierungsstellen, zur Unterstützung bei Auditierungsprozessen.
Wie hoch sind die Kosten für eine ISO 13485-Zertifizierung?
Die Kosten der ISO 13485-Zertifizierung können stark variieren und hängen von mehreren Faktoren ab, darunter die Größe der Organisation, die Komplexität der Medizinprodukte und die spezifischen Anforderungen des regulatorischen Umfelds.
Welche Dokumentation ist für die ISO 13485-Zertifizierung erforderlich?
Um die ISO 13485-Zertifizierung zu erreichen, müssen Sie verschiedene Dokumente vorbereiten. Dazu gehören:
-
Qualitätsmanagement-Handbuch.
-
Qualitätspolitik und Verfahrensanweisungen.
-
Prozesse zur Softwarevalidierung.
-
Medizinprodukteakte.
-
Aufzeichnungen über die Mitwirkung des Managements.
-
Mitarbeiterunterlagen.
-
Aufzeichnungen zu Infrastruktur und Wartung.
-
Maßnahmen zur Kontaminationskontrolle.
Wie lange dauert es, die ISO 13485-Zertifizierung zu erhalten?
Die Zeitspanne bis zum Erhalt der ISO 13485-Zertifizierung kann variieren, beträgt aber im Allgemeinen zwischen 6 und 9 Monaten. Dieser Zeitrahmen kann sich aufgrund der Verfügbarkeit von Auditoren der Benannten Stellen (Notified Bodies) oder Zertifizierungsstellen, die für die Durchführung und Bestätigung des Audits erforderlich sind, verlängern. Es ist entscheidend, diese Organisationen so früh wie möglich einzubinden, um eine rechtzeitige Terminierung des Vor-Ort-Audits sicherzustellen.
About the Author
Jonathan
Jonathan Sternberg, founder of Sternberg Consulting, brings extensive experience from the automotive, semiconductor, and optical industries. He focuses on customized solutions and genuine collaboration in quality management.